乙醇发表评论(0)编辑词条
乙醇 
分子立体模型概述
乙醇的分子式为CH3CH2OH,俗称酒精,它在常温、常压下是一种易燃、易挥发的无色透明液体,它的水溶液具有特殊的、令人愉快的香味,并略带刺激性。乙醇的用途很广,可用乙醇来制造醋酸、饮料、香精、染料、燃料等。医疗上也常用体积分数为70%——75%的乙醇作消毒剂等。
中文名称: 乙醇 ; 酒精
英文名称: ethyl alcohol ; ethanol
分子式:C2H6O
结构简式:CH3CH2OH或C2H5OH
官能团:羟基(-OH)
CAS 登录号:64-17-5
EINECS 登录号:200-578-6
RTECS号: KQ6300000
化学式:C2H5OH,C2H6O,CH3CH2OH
(结构如右图)C、O原子均以sp3杂化轨道成键、极性分子。乙醇结构
描述:乙醇分子是由乙基和羟基两部分组成,可以看成是乙烷分子中的一个氢原子被羟基取代的产物,也可以看成是水分子中的一个氢原子被乙基取代的产物。乙醇分子中的碳氧键和氢氧键比较容易断裂。
相对分子量: 46.07
性质
MolarMass = 46.06844(232)
外观与性状: 无色液体,有特殊香味。
密度:0.789 g/cm^3; (液)
熔点:−117.3 °C (158.8 K)
沸点:78.5 °C (351.6 K)
在水中的溶解度:pKa 15.9
黏度:1.200 mPa·s (cP), 20.0 °C
分子偶极矩:5.64 fC·fm (1.69 D) (气)
折射率:1.3614
相对密度(水=1): 0.79
相对蒸气密度(空气=1): 1.59
饱和蒸气压(kPa): 5.33(19℃)
燃烧热(kJ/mol): 1365.5
临界温度(℃): 243.1
临界压力(MPa): 6.38
辛醇/水分配系数的对数值: 0.32
闪点(℃): 12
引燃温度(℃): 363
爆炸上限%(V/V): 19.0
爆炸下限%(V/V): 3.3
溶解性: 与水混溶,可混溶于醚、氯仿、甘油等多数有机溶剂。
电离性:非电解质
无色、透明,具有特殊香味的液体(易挥发),密度比水小,能跟水以任意比互溶(一般不能做萃取剂)。是一种重要的溶剂,能溶解多种有机物和无机物。
物理性质
乙醇的物理性质主要与其低碳直链醇的性质有关。分子中的羟基可以形成氢键,因此乙醇黏度[1]很大,也不及相近相对分子质量的有机化合物极性大。室温下,乙醇是无色易燃,且有特殊香味的挥发性液体。
λ=589.3nm和18.35°C下,乙醇的折射率为1.36242,比水稍高。
作为溶剂,乙醇易挥发,且可以与水、乙酸、丙酮、苯、四氯化碳、氯仿、乙醚、乙二醇、甘油、硝基甲烷、吡啶和甲苯等溶剂混溶。此外,低碳的脂肪族烃类如戊烷和己烷,氯代脂肪烃如1,1,1-三氯乙烷和四氯乙烯也可与乙醇混溶。随着碳数的增长,高碳醇在水中的溶解度明显下降。
由于存在氢键,乙醇具有潮解性,可以很快从空气中吸收水分。羟基的极性也使得很多离子化合物可溶于乙醇中,如氢氧化钠、氢氧化钾、氯化镁、氯化钙、氯化铵、溴化铵和溴化钠等。氯化钠和氯化钾则微溶于乙醇。此外,其非极性的烃基使得乙醇也可溶解一些非极性的物质,例如大多数香精油和很多增味剂、增色剂和医药试剂。
化学性质
酸性
乙醇分子中含有极化的氧氢键,电离时生成烷氧基负离子和质子。
CH3CH2OH→(可逆)CH3CH2O- + H+
乙醇的pKa=15.9,与水相近。
乙醇的酸性很弱,但是电离平衡的存在足以使它与重水之间的同位素交换迅速进行。
CH3CH2OH+D2O→(可逆)CH3CH2OD+HOD
因为乙醇可以电离出极少量的氢离子,所以其只能与少量金属(主要是碱金属)反应生成对应的醇金属以及氢气:
2CH3CH2OH + 2Na→2CH3CH2ONa + H2
醇金属遇水则迅速水解生成醇和碱
结论:
(1)乙醇可以与金属钠反应,产生氢气,但不如水与金属钠反应剧烈。
(2)活泼金属(钾、钙、钠、镁、铝)可以将乙醇羟基里的氢取代出来。
与乙酸反应
乙醇可以与乙酸在浓硫酸的催化并加热的情况下发生酯化作用,生成乙酸乙酯。
CH3CH2OH + CH3COOH →CH3COOCH2CH3 + H2O
与氢卤酸反应
C2H5OH + HBr→C2H5Br + H2O
C2H5OH + HX→C2H5X + H2O
注意:通常用溴化钠和硫酸的混合物与乙醇加热进行该反应。故常有红棕色气体产生。
氧化反应
(1)燃烧:发出淡蓝色火焰,放出大量的热
C2H5OH+3O2→2CO2+3H2O
(2)催化氧化:在加热和有催化剂(Cu或Ag)存在的情况下进行。
2CH3CH2OH+O2→2CH3CHO+2H2O (工业制乙醛)
C2H5OH+CuO→CH3CHO+Cu+H2O
即催化氧化的实质(用Cu作催化剂)
消去反应
(1)分子内消去制乙烯(170℃浓硫酸)
C2H5OH→C2H4+H2O
(2)分子间消去制乙醚(140℃ 浓硫酸)
C2H5OH + HOC2H5 →C2H5OC2H5 + H2O(此为取代反应)
酯化反应
C2H5OH+CH3COOH-浓H2SO4△(可逆)→CH3COOCH2CH3+H2O
“酸”脱“羟基”,“醇”脱“氢”
燃烧
乙醇可以与空气中氧气发生剧烈的氧化反应产生燃烧现象,生成水和二氧化碳。
CH3CH2OH+3O2 → 2CO2+3H2O
乙醇也可被浓硫酸跟高锰酸钾的混合物发生非常激烈的氧化反应,燃烧起来。
与卤化氢反应
乙醇可以和卤化氢发生取代反应,生成卤代烃和水。例如:
CH3CH2OH + HBr → CH3CH2Br + H-OH
脱水反应
乙醇可以在浓硫酸和高温的催化发生脱水反应,随着温度的不同生成物也不同。
如果温度在140℃左右生成物是乙醚
CH3CH2-OH + HO-CH2CH3 → CH3CH2OCH2CH3 + H2O
如果温度在170℃左右,生成物为乙烯
CH2HCH2OH →CH2=CH2 + H2O
还原性
乙醇具有还原性,可以被氧化成为乙醛。酒精中毒的罪魁祸首通常被认为是有一定毒性的乙醛,而并非喝下去的乙醇。例如
2CH3CH2OH + O2 → 2CH3CHO + 2H2O(条件是在催化剂的作用下加热)
与活泼金属反应乙醇可以和高活跃性金属反应,生成醇盐和氢气。例如与钠的反应:
2CH3CH2OH + 2Na → 2CH3CH2ONa + H2
健康
用途
乙醇的用途很广,主要有: 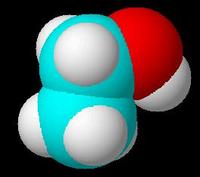
(1)消毒剂:
医院用的一般用浓度为70%~75%的乙醇溶液,因为这种浓度的乙醇溶液杀菌能力最强;
此外也是碘酒消毒剂的成分之一。
(2)饮料:
乙醇是酒主要成分(含量和酒的种类有关系)如白酒为56度的酒。注意:我们喝的酒内的乙醇不是把乙醇加进去,而是发酵出来的乙醇,当然根据使用的发酵酶不同还会有乙酸或糖等有关物质。
(3)基本有机化工原料:
乙醇可用来制取乙醛、乙醚、乙酸乙酯、乙胺等化工原料,也是制取、染料、涂料、洗涤剂等产品的原料
(4)汽车燃料:
乙醇可以调入汽油,作为车用燃料,美国销售乙醇汽油已有20年历史。
此外乙醇还做:稀释剂、有机溶剂、涂料溶剂等几大方面,其中用量最大的是消毒剂。
工业制法
工业上一般用淀粉发酵法或乙烯的水化法制取乙醇:
1.淀粉发酵法
2.乙烯水化法
CH2═CH2 + H─OH→C2H5OH(该反应分两步进行,第一步是与醋酸汞等汞盐在水-四氢呋喃溶液中生成有机汞化合物,而后用硼氢化钠还原)
[编辑本段]危险性
EU分类 可燃 (F)
警示性质标准词 R11
安全建议标准词 S2, S7, S16
闪点 286.15 K (13 °C or 55.4 °F)
毒性:LD50 85 mg/kg
健康危害: 本品为中枢神经系统抑制剂。首先引起兴奋,随后抑制。急性中毒:急性中毒多发生于口服。一般可分为兴奋、催眠、麻醉、窒息四阶段。患者进入第三或第四阶段,出现意识丧失、瞳孔扩大、呼吸不规律、休克、心力循环衰竭及呼吸停止。慢性影响:在生产中长期接触高浓度本品可引起鼻、眼、粘膜刺激症状,以及头痛、头晕、疲乏、易激动、震颤、恶心等。长期酗酒可引起多发性神经病、慢性胃炎、脂肪肝、肝硬化、心肌损害及器质性精神病等。皮肤长期接触可引起干燥、脱屑、皲裂和皮炎。 乙醇具有成瘾性及致癌性,但乙醇并不是直接导致癌症的物质,而是致癌物质普遍溶于乙醇。在中国传统医药观点上,乙醇有促进人体吸收药物的功能,并能促进血液循环,治疗虚冷症状。药酒便是依照此原理制备出来的
燃爆危险: 本品易燃,具刺激性。
危险特性: 易燃,其蒸气与空气可形成爆炸性混合物,遇明火、高热能引起燃烧爆炸。与氧化剂接触发生化学反应或引起燃烧。在火场中,受热的容器有爆炸危险。其蒸气比空气重,能在较低处扩散到相当远的地方,遇火源会着火回燃。
急救:
皮肤接触: 脱去污染的衣着,用肥皂水和清水彻底冲洗皮肤。
眼睛接触:提起眼睑,用流动清水或生理盐水冲洗。就医。
吸入:迅速脱离现场至空气新鲜处。保持呼吸道通畅。如呼吸困难,给输氧。如呼吸停止,立即进行人工呼吸。就医。
食入: 饮足量温水,催吐。就医。
防护措施
工程控制: 密闭操作,加强通风
呼吸系统防护: 空气中浓度较高时,应该佩戴自吸过滤式防尘口罩。必要时,建议佩戴自给式呼吸器
眼睛防护: 戴化学安全防护眼镜。
身体防护: 穿胶布防毒衣。
手防护: 戴橡胶手套。
其他防护: 工作完毕,淋浴更衣。保持良好的卫生习惯。
吸收与代谢
乙醇的吸收:
饮酒后,乙醇很快通过胃和小肠的毛细血管进入血液。一般情况下,饮酒者血液中乙醇的浓度(blood alcohol concentration,BAC)在30~45分钟内将达到最大值,随后逐渐降低。当BAC超过1000mg/L时,将可能引起明显的乙醇中毒。摄入体内的乙醇除少量未被代谢而通过呼吸和尿液直接排出外,大部分乙醇需被氧化分解。
乙醇的代谢:
在乙醇的代谢过程中乙醇脱氢酶(alcohol dehydrogenase,ADH)起着至关重要的作用,它主要分布在肝脏,在胃肠道及其他组织中也有少量分布。乙醇通过血液流到肝脏后,首先被ADH氧化为乙醛,而乙醛脱氢酶则能把乙醛中的两个氢原子脱掉,分解为二氧化碳和水,在肝脏中乙醇还能被CYP2E1酶分解代谢。
人喝酒后面部潮红,是因为皮下暂时性血管扩张所致,因为这些人体内有高效的乙醇脱氢酶,能迅速将血液中的酒精转化成乙醛,而乙醛具有让毛细血管扩张的功能,会引起脸色泛红甚至身上皮肤潮红等现象,也就是我们平时所说的“上脸”。
乙醇代谢的速率主要取决于体内酶的含量,其具有较大的个体差异,并与遗传有关。人体内若是具备这两种酶,就能较快地分解酒精,中枢神经就较少受到酒精的作用,因而即使喝了一定量的酒后,也行若无事。在人体中,都存在乙醇脱氢酶,而且大部分人数量基本是相等的。但缺少乙醛脱氢酶的人就比较多。这种乙醛脱氢酶的缺少,使酒精不能被完全分解为水和二氧化碳,而是以乙醛继续留在体内。你所说的酒精的代谢应该是被完整的分解后的状态,由于很多人缺少乙醛脱氢酶,拥有乙醛脱氢酶的量也是有差别的,所以严格的说酒精的代谢速度是没法用一个准确的速度来描述的,因人而异。
包装与储运
包装方法: 两层塑料袋或一层塑料袋外麻袋、塑料编织袋、乳胶布袋;塑料袋外复合塑料编织袋(聚丙烯三合一袋、聚乙烯三合一袋、聚丙烯二合一袋、聚乙烯二合一袋);螺纹口玻璃瓶、铁盖压口玻璃瓶、塑料瓶或金属桶(罐)外普通木箱;螺纹口玻璃瓶、塑料瓶或镀锡薄钢板桶(罐)外满底板花格箱、纤维板箱或胶合板箱。
包装类别: O53
包装标志: 有毒品
储运注意事项: 铁路运输时应严格按照铁道部《危险货物运输规则》中的危险货物配装表进行配装。运输时单独装运,运输过程中要确保容器不泄漏、不倒塌、不坠落、不损坏。运输时运输车辆应配备相应品种和数量的消防器材。严禁与酸类、易燃物、有机物、还原剂、自燃物品、遇湿易燃物品等并车混运。运输时车速不宜过快,不得强行超车。运输车辆装卸前后,均应彻底清扫、洗净,严禁混入有机物。储存于阴凉、通风的库房。远离火种、热源。库温不超过30℃,相对湿度不超过80%。包装要求密封,不可与空气接触。应与还原剂、活性金属粉末、酸类、食用化学品分开存放,切忌混储。储区应备有合适的材料收容泄漏物。
[编辑本段]泄漏处置和废弃
泄漏处置方法: 隔离泄漏污染区,限制出入。建议应急处理人员戴防尘面具(全面罩),穿防毒服。勿使泄漏物与还原剂、有机物、易燃物或金属粉末接触。不要直接接触泄漏物。小量泄漏:用洁净的铲子收集于干燥、洁净、有盖的容器中。大量泄漏就收集回收或运至废物处理场所处置。
废弃方法: 根据国家和地方有关法规的要求处置。或与厂商或制造商联系,确定处置方法。
乙醇和甲醇的区别
甲醇是甲烷的一个氢原子被羟基(一个氢和一个氧组成的原子团,不是氢氧根)替换后的产物。
乙醇是乙烷一个氢原子被羟基替换后的产物,俗称酒精。
分子是不一样。
甲烷:
甲醇:
甲醇结构
乙醇:
乙醇结构
他们的分子式不一样,化学性质和物理性质也有区别。
乙醇密度表
乙醇溶液密度(g/cm3)(20℃)-每(g/cm3)含有乙醇重量(%)g-浓度(体积比%)=度(1度=1%体积)
0.998-0.15-0.2
0.996-1.20-1.5
0.994-2.30-3.0
0.992-3.50-4.4
0.990-4.70-5.9
0.988-5.90-7.4
0.985-7.90-9.9
0.982-10.0-12.5
0.980-11.5-14.2
0.978-13.0-16.0
0.975-15.3-18.9
0.972-17.6-21.7
0.970-19.1-23.5
0.968-20.6-25.3
0.965-22.8-27.8
0.962-24.8-30.3
0.960-26.2-31.8
0.957-28.1-34.0
0.954-29.9-36.1
0.950-32.2-38.8
0.945-35.0-41.3
0.940-37.6-44.8
0.935-40.1-47.5
0.930-42.6-50.2
0.925-44.9-52.7
0.920-47.3-55.1
0.915-49.5-57.4
0.910-51.8-59.7
0.905-53.9-61.9
0.900-56.2-64.0
0.895-58.3-66.2
0.890-60.5-68.2
0.885-62.7-70.2
0.880-64.8-72.2
0.875-66.9-74.2
0.870-69.0-76.1
0.865-71.1-77.9
0.860-73.2-79.7
0.855-75.3-81.5
0.850-77.3-83.3
0.845-79.4-85.0
0.840-81.4-86.6
0.835-83.4-88.2
0.830-85.4-89.8
0.825-87.3-91.2
0.820-89.2-92.7
0.815-91.1-94.1
0.810-93.0-95.4
0.805-94.4-96.6
0.800-96.5-97.7
0.795-98.2-98.9
0.791-99.5-99.7
从中可以计算出:每(g/cm3)含有乙醇重量(%)g
浓度(体积比%)=度(1度=1%体积)
例如:密度为0.791g/cm3
每(g/cm3)含有乙醇重量:0.791×99.5%=0.787045g
浓度:99.7%=99.7度
健康
酒精(乙醇)具有成瘾性及致癌性,但乙醇并不是直接导致癌症的物质,而是致癌物质普遍溶于乙醇。有机会会有癌症和上瘾。
在中国传统医药观点上,乙醇有促进人体吸收药物的功能,并能促进血液循环,治疗虚冷症状。药酒便是依照此原理制备出来的。
漱口水如果含有较高浓度的酒精,就算不吞入也可能有害健康。
与“乙醇,化工”相关的词条
→如果您认为本词条还有待完善,请 编辑词条
词条内容仅供参考,如果您需要解决具体问题
(尤其在法律、医学等领域),建议您咨询相关领域专业人士。
0

同义词: 暂无同义词
关于本词条的评论 (共0条)发表评论>>







