氧化铁发表评论(0)编辑词条
化学性质编辑本段回目录
物理性质编辑本段回目录
式量:160
性状:红棕色粉末
相对密度(水=1):5.24
熔点:1565℃
稳定性:稳定,溶于盐酸、稀硫酸生成+3价铁盐。
溶解性:不溶于水,不与水反应。
氧化性:(高温下)被CO、H2、Al、C、Si等还原。
存在形式:矿物:赤铁矿、赭石
别名:三氧化二铁、铁红、铁丹、赤铁矿、铁锈
三氧化二铁是铁锈*(原理见制法)的主要成分。
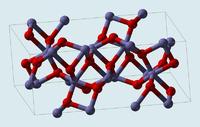
来源于维基百科
α型晶胞结构:编辑本段回目录
CAS Registry Number:编辑本段回目录
1309-37-1
4Fe+6H20+3O2=4Fe(OH)3
在空气中灼烧亚铁化合物或氢氧化铁等可得三氧化二铁。
在潮湿的空气中,钢铁表面吸附了一层薄薄的水膜,这层水膜里含有少量的H+和OH-,还溶解了氧气,结果在钢铁表面形成了一层电解质溶液,它跟钢铁里的铁和少量的碳(因钢铁不纯)恰好形成无数微小的原电池。在这些原电池里,铁是负极,碳是正极。铁失去电子而被氧化:
负极:2Fe-4e-=2Fe2+
正极:2H2O+O2+4e-=4OH-
电化学腐蚀是造成钢铁腐蚀的主要原因。
在此之后继续反应:
Fe2+2OH-=Fe(OH)2
4Fe(OH)2+O2+2H2O=4Fe(OH)3
2Fe(OH)3+nH2O=2Fe2O3。nH2O+3H2O
在初中的化学里,可用盐酸(HCl)来除铁锈。
方程式为:Fe2O3+6HCl=2FeCl3+3H2O
1. 其红棕色粉末为一种低级颜料,工业上称氧化铁红,用于油漆、油墨、橡胶等工业中
2. 可做催化剂
4.用于和CO反应炼制生铁(H2也可) Fe2O3+3CO=2Fe+3CO2(高温) Fe2O3+3H2=2Fe+3H2O(高温) 2Fe2O3+3C=4Fe+3CO2(气)(高温)
参见铁的其它氧化物:氧化亚铁、四氧化三铁(在氧气中剧烈燃烧生成)化学方程式:3Fe+2O2=点燃=Fe3O4
制法
4Fe+6H20+3O2=4Fe(OH)3
在空气中灼烧亚铁化合物或氢氧化铁等可得三氧化二铁。
在潮湿的空气中,钢铁表面吸附了一层薄薄的水膜,这层水膜里含有少量的H+和OH-,还溶解了氧气,结果在钢铁表面形成了一层电解质溶液,它跟钢铁里的铁和少量的碳(因钢铁不纯)恰好形成无数微小的原电池。在这些原电池里,铁是负极,碳是正极。铁失去电子而被氧化:
负极:2Fe-4e-=2Fe2+
正极:2H2O+O2+4e-=4OH-
电化学腐蚀是造成钢铁腐蚀的主要原因。
在此之后继续反应:
Fe2+2OH-=Fe(OH)2
4Fe(OH)2+O2+2H2O=4Fe(OH)3
2Fe(OH)3+nH2O=2Fe2O3。nH2O+3H2O
在初中的化学里,可用盐酸(HCl)来除铁锈。
方程式为:Fe2O3+6HCl=2FeCl3+3H2O
用途
1. 其红棕色粉末为一种低级颜料,工业上称氧化铁红,用于油漆、油墨、橡胶等工业中
2. 可做催化剂
3. 玻璃、宝石、金属的抛光剂
4.用于和CO反应炼制生铁(H2也可) Fe2O3+3CO=2Fe+3CO2(高温) Fe2O3+3H2=2Fe+3H2O(高温) 2Fe2O3+3C=4Fe+3CO2(气)(高温)
参见铁的其它氧化物:氧化亚铁、四氧化三铁(在氧气中剧烈燃烧生成)化学方程式:3Fe+2O2=点燃=Fe3O4
与“氧化铁,铁锈”相关的词条
→如果您认为本词条还有待完善,请 编辑词条
词条内容仅供参考,如果您需要解决具体问题
(尤其在法律、医学等领域),建议您咨询相关领域专业人士。
0
收藏到: 

同义词: 暂无同义词
关于本词条的评论 (共0条)发表评论>>








